Cerveau
Tumeurs cérébrales
Traitement des Tumeurs Cérébrales à Pau : Expertise en Neurochirurgie dans les Pyrénées
Le traitement des tumeurs cérébrales à Pau est assuré par une équipe de neurochirurgiens spécialisés, offrant des soins de pointe aux patients des départements 64 (Pyrénées-Atlantiques) et 65 (Hautes-Pyrénées). Grâce à des technologies médicales avancées et à une approche multidisciplinaire, ces experts en neurochirurgie diagnostiquent et traitent une variété de tumeurs cérébrales, qu’elles soient bénignes ou malignes.
Les tumeurs cérébrales, qui peuvent affecter diverses fonctions du cerveau en fonction de leur emplacement, nécessitent une prise en charge rapide et précise. À Pau, les neurochirurgiens utilisent des techniques sophistiquées telles que la chirurgie assistée par ordinateur, la neuronavigation et l’imagerie peropératoire pour localiser et retirer les tumeurs avec la plus grande précision possible. Ces technologies permettent de minimiser les risques de lésions aux tissus sains environnants.
Le Centre Hospitalier de Pau, ainsi que des cliniques privées, offrent des infrastructures de haut niveau pour le traitement des tumeurs cérébrales. Les patients de la région des Pyrénées bénéficient d’un accès à des soins neurochirurgicaux de qualité sans avoir à se déplacer loin de chez eux, facilitant ainsi le suivi médical et la rééducation post-opératoire. En plus de la chirurgie, d’autres options thérapeutiques telles que la radiothérapie ou la chimiothérapie peuvent être proposées en fonction de la nature de la tumeur.
Les neurochirurgiens de Pau travaillent en étroite collaboration avec des oncologues, neurologues et radiologues pour offrir une prise en charge complète et personnalisée. Cette approche permet de maximiser les chances de réussite du traitement et d’améliorer la qualité de vie des patients atteints de tumeurs cérébrales.
Les habitants des Pyrénées, qu’ils soient de Pau, Bayonne ou Tarbes, peuvent donc compter sur un accompagnement médical d’excellence pour le traitement des tumeurs cérébrales, tout en restant dans leur région.

Ce chapitre est destiné principalement aux patients. Certaines informations médicales peuvent être légèrement simplifiées pour permettre la compréhension du grand public.
Définition
Le développement anormal de cellules dans le corps humain s’appelle une tumeur. On distingue les tumeurs dites bénignes (non agressives) des tumeurs dites malignes (agressives).
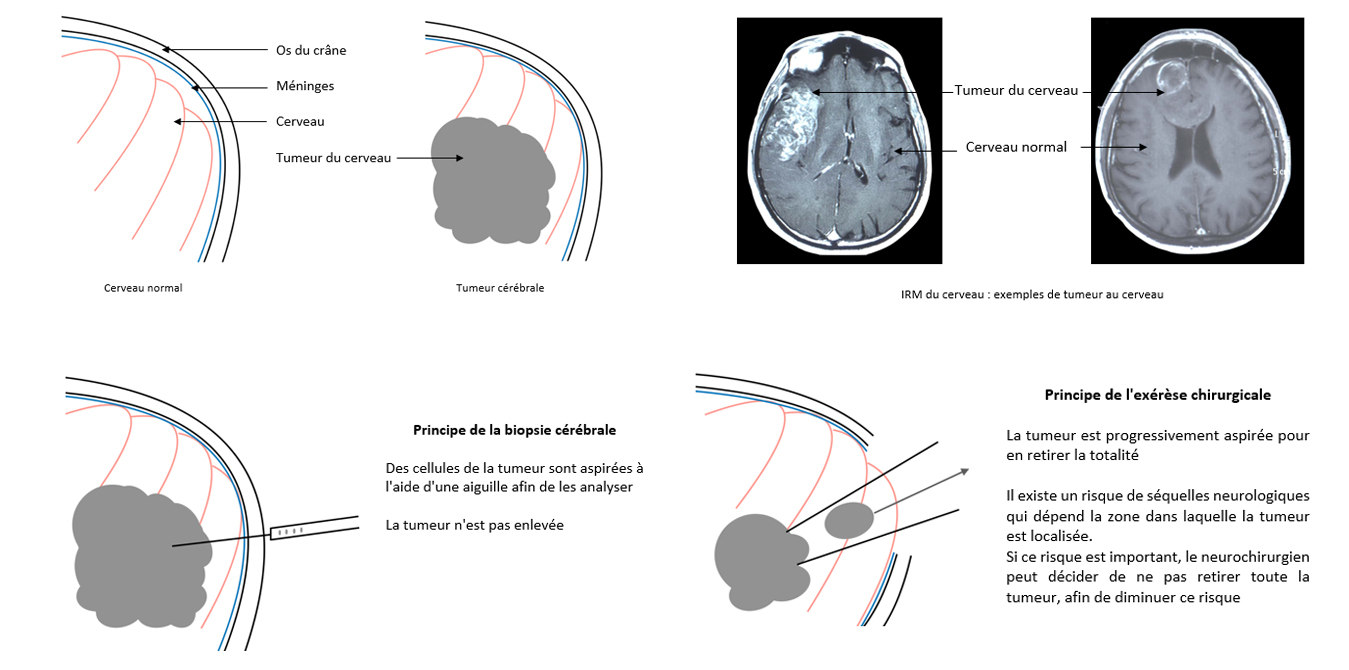
Les tumeurs du cerveau, ou tumeurs cérébrales, correspondent donc à un développement anormal de cellules du cerveau. Les cellules s’accumulent progressivement (d’autant plus vite que la tumeur est agressive) et finissent par former une masse au sein du cerveau. Cette masse va comprimer le cerveau normal et l’empêcher de fonctionner normalement.
Les tumeurs cérébrales peuvent concerner tous les types de cellules composant le cerveau. Il existe donc une multitude de type de tumeur cérébrale. Ces tumeurs peuvent être bénignes ou malignes. La tumeur cérébrale la plus fréquente est appelée glioblastome. L’ensemble de toutes les tumeurs cérébrales représente 1% de l’ensemble des tumeurs pouvant affecter l’organisme.
La cause du développement d’une tumeur cérébrale n’est pas connue de manière précise. Elles sont la plupart du temps non héréditaires.
Contrairement à la plupart des autres tumeurs pouvant se développer dans le corps, les tumeurs cérébrales ne peuvent pas envoyer de cellules malades hors du système nerveux (cerveau, moelle épinière et nerfs). Autrement dit, elles ne donnent jamais de métastase dans le reste du corps.
Symptômes et signes cliniques
Les symptômes liés aux tumeurs cérébrales sont très variables selon la localisation et le volume de la tumeur cérébrale. Du fait de la croissance progressive des tumeurs, les symptômes ont tendance à s’aggraver progressivement, en quelques semaines pour les tumeurs agressives et en quelques mois/années pour les tumeurs peu agressives.
Le développement progressif d’une tumeur au sein du cerveau va entrainer une augmentation progressive de la pression au sein de la boite crânienne, appelée hypertension intracrânienne. Cette dernière entraine essentiellement des maux de tête (céphalées), des nausées et vomissements, et des troubles de la vision (vision double, flou visuel). Ces symptômes s’aggravent d’autant plus vite que la tumeur grossit vite.
La tumeur peut être localisée dans une zone importante du cerveau (dite fonctionnelle) et ainsi empêcher cette zone de fonctionner correctement. On parle de déficit neurologique focal. Par exemple, une tumeur située en regard de la zone du cerveau qui commande les mouvements du bras droit peut entrainer une paralysie progressive du bras droit. Ces symptômes sont très variables selon la localisation de la tumeur au sein de la boite crânienne. Si la tumeur est située à distance des zones dites fonctionnelles, aucun déficit neurologique focal ne sera observé.
La tumeur peut également entrainer des crises d’épilepsie. Elles sont liées à une irritation du cerveau par la tumeur. Il existe 2 grands types de crises d’épilepsie à savoir les crises dites focales et les crises dites généralisées. Les crises focales correspondent à un déficit neurologique focal transitoire de quelques minutes avec récupération complète après la crise (ex : paralysie du bras droit pendant 20 min). Les crises généralisées correspondent à une perte de connaissance avec des mouvements des 4 membres. Une tumeur peut entrainer des crises focales, des crises généralisées ou les 2.
Enfin, certaines tumeurs peu agressives et de petite taille n’entrainent la plupart du temps aucun symptôme, et peuvent être découvertes par hasard lors de la réalisation d’un examen de radiologie réalisé pour un autre motif.
Bilans complémentaires à réaliser
Le diagnostic de tumeur cérébrale doit être confirmé par des examens de radiologie permettant de mettre en évidence une masse au sein du cerveau.
Les radiographies du crâne et/ou de la colonne vertébrale n’ont que très peu d’intérêt car elles ne permettent pas de voir les méninges.
Les 2 examens permettant de visualiser une tumeur sont le scanner et l’IRM du cerveau. L’IRM permet d’analyser le cerveau de manière plus précise que le scanner et est donc considérée comme l’examen de référence à réaliser.
Prise en charge
La prise en charge d’une tumeur cérébrale est dite multidisciplinaire, car elle fait intervenir plusieurs types de médecins spécialistes (cancérologue, anatomopathologiste neurologue, neuroradiologue, neurochirurgien, radiothérapeute). Chaque cas de probable tumeur du cerveau est discuté en réunion multidisciplinaire, organisée avec l’équipe de radiothérapie et d’oncologie (GROP, qui regroupe les centres situés à Pau (Clinique Marzet) et à Tarbes (Clinique de l’Ormeau)).
Le traitement d’une tumeur cérébrale dépend du type exact de la tumeur. Il existe une multitude de type de tumeurs. Les examens de radiologie ne permettent pas de les préciser de manière exacte. A l’heure actuelle, le seul moyen de définir avec certitude le type de tumeur cérébrale est l’analyse au microscope de cellules provenant de la tumeur. Ces cellules pourront être obtenues en pratiquant une intervention chirurgicale.
Ainsi, sauf cas exceptionnel, une intervention chirurgicale devra être réalisée devant une suspicion de tumeur cérébrale. La chirurgie réalisée peut être soit une biopsie, soit une exérèse. Le choix du type de chirurgie est réalisé par le neurochirurgien. La chirurgie est toujours réalisée sous anesthésie générale.
La biopsie consiste à prélever avec une aiguille des cellules de la tumeur. Elle permet ainsi d’envoyer des cellules au laboratoire pour analyse et obtention du type de tumeur. Elle a l’avantage d’être une chirurgie rapide et bien tolérée par le patient. L’inconvénient vient du fait que la tumeur n’est pas enlevée.
La biopsie de la lésion est réalisée avec une assistance informatique appelée neuronavigation. L’équipe de neurochirurgie de la polyclinique Pau Pyrénées dispose de la nouvelle neuronavigation Brainlab© avec un nouveau système de visée spécifique. La polyclinique Pau Pyrénées est le premier centre en France à être équipé de ce nouveau système.
L’exérèse chirurgicale consiste à retirer le plus possible de tumeur (toute la tumeur dans la mesure du possible). Elle permet ainsi d’envoyer des cellules au laboratoire pour analyse et obtention du type de tumeur. L’inconvénient de ce type de chirurgie vient du fait qu’elle est plus lourde pour le patient qu’une simple biopsie, et qu’il existe un risque plus important de séquelles neurologiques après l’intervention.
L’équipe de neurochirurgie de la polyclinique Pau Pyrénées dispose de nombreux moyens de limiter les risques de séquelles neurologiques après l’intervention. L’utilisation de la neuronavigation permet au neurochirurgien d’identifier très précisément la zone du cerveau dans laquelle se situe la tumeur. L’utilisation de produits fluorescents peut permettre d’identifier la tumeur au sein du cerveau normal pendant l’opération. L’utilisation du dissecteur ultrasonique cérébral permet de limiter nettement le risque de lésion du cerveau sain pendant l’intervention. L’utilisation d’un neurostimulateur permet également de tester le fonctionnement du cerveau pendant l’intervention et de décider quelles zones devront être préservées.
Par exemple, si la tumeur est située près de la zone du cerveau qui commande la main droite, il existe un risque de ne plus pouvoir bouger la main droite après l’opération. Lorsque le neurochirurgien placera le neurostimulateur sur la zone du cerveau responsable de ce mouvement, la main du patient ne pourra plus bouger. La zone stimulée sera préservée (même si elle contient de la tumeur) afin que le patient n’ait pas de séquelle au niveau de la main droite.
Une fois la chirurgie réalisée et le diagnostic précis du type de tumeur obtenu, un traitement complémentaire pourra être réalisé. L’intérêt d’un traitement complémentaire est discuté de manière pluridisciplinaire (entre neurochirurgien, oncologue, radiothérapeute, anatomopathologiste et neuroradiologue). Il dépend de l’agressivité de la tumeur et de la chirurgie réalisée. Ce traitement comporte principalement des médicaments (chimiothérapie) et/ou de la radiothérapie.
La radiothérapie consiste à envoyer, par le biais d’une machine, des rayons sur la tumeur pour en détruire les cellules.
La chimiothérapie consiste à administrer des médicaments qui vont aller détruire les cellules de la tumeur.
Dans tous les cas, un suivi régulier avec une IRM cérébrale est nécessaire pendant plusieurs années (et souvent à vie), même en cas de tumeur considérée comme guérie.
Tumeurs méningées sous-élément
Traitement des Tumeurs Cérébrales dans le 64 : Expertise en Neurochirurgie à Pau et dans les Pyrénées
Dans les Pyrénées-Atlantiques (64) et les Hautes-Pyrénées (65), les neurochirurgiens spécialisés de Pau offrent des solutions de pointe pour le traitement des tumeurs cérébrales. Ces pathologies, qu’elles soient bénignes ou malignes, nécessitent une prise en charge rapide et experte en raison des risques qu’elles posent pour la santé neurologique des patients.
Les tumeurs cérébrales peuvent entraîner divers symptômes en fonction de leur localisation, tels que des maux de tête persistants, des troubles visuels, des difficultés motrices ou encore des pertes de mémoire. Grâce aux infrastructures médicales modernes disponibles à Pau, notamment au Centre Hospitalier de Pau et dans les cliniques privées de la région, les patients bénéficient d’un accès à des technologies de pointe pour le diagnostic et le traitement de ces affections complexes.
Les neurochirurgiens de Pau utilisent des techniques chirurgicales avancées comme la neuronavigation, l’imagerie intra-opératoire et la chirurgie guidée par ordinateur. Ces outils permettent d’opérer avec une extrême précision, minimisant ainsi les risques pour les tissus cérébraux sains et optimisant les chances de retirer la totalité de la tumeur. En fonction de la nature de la tumeur, ces interventions peuvent être combinées avec des traitements complémentaires comme la radiothérapie ou la chimiothérapie, assurant une prise en charge globale et personnalisée.
Les patients résidant dans le 64 et le 65, que ce soit à Pau, Bayonne, Tarbes ou Lourdes, peuvent ainsi recevoir des soins neurochirurgicaux de haute qualité près de chez eux, évitant des déplacements vers de grandes métropoles. Ce suivi local permet une meilleure coordination entre les différents spécialistes, garantissant un accompagnement optimal tout au long du processus de traitement.
Grâce à l’expertise en neurochirurgie dans les Pyrénées, les patients atteints de tumeurs cérébrales peuvent espérer une meilleure qualité de vie et une prise en charge adaptée à leurs besoins.

Ce chapitre est destiné principalement aux patients. Certaines informations médicales peuvent être légèrement simplifiées pour permettre la compréhension du grand public.
Par définition, les méninges constituent des membranes qui entourent le cerveau, la moelle épinière et certains nerfs. Ces méninges se répartissent en 3 couches successives, à savoir la dure-mère, l’arachnoïde et la pie-mère (de l’extérieur vers l’intérieur). L’ensemble de ces 3 couches est extrêmement fin (1mm).
Au niveau de la tête, les méninges sont situées entre le cerveau (à l’intérieur) et les os du crâne (à l’extérieur). Au niveau de la colonne vertébrale, les méninges sont situées entre la moelle épinière/queue de cheval (à l’intérieur) et les vertèbres (à l’extérieur).
Le développement anormal de cellules dans le corps humain s’appelle une tumeur. On distingue les tumeurs dites bénignes (non agressives) des tumeurs dites malignes (agressives).
Les tumeurs des méninges les plus fréquentes sont les méningiomes (plus de 95% des cas). Ils correspondent à une accumulation anormale de cellules au niveau de l’arachnoïde. Ceci va d’abord entrainer un épaississement de cette membrane, puis la formation d’une véritable masse de cellules. Cette masse se développe donc en dehors du cerveau ou de la moelle épinière/queue de cheval. De par sa localisation, cette masse peut entrainer une compression du cerveau (pour les méningiomes crâniens) ou de la moelle épinière/queue de cheval (pour les méningiomes de la colonne vertébrale).
Les méningiomes sont plus fréquents au niveau du crâne que de la colonne vertébrale, ainsi que chez les femmes. Ce sont dans la plupart des cas des tumeurs bénignes, dont la croissance très lente se fait sur plusieurs mois/années.
La cause du développement d’un méningiome n’est pas connue de manière précise. Certains méningiomes peuvent être lien à la prise de médicaments hormonaux.
Symptômes et signes cliniques
Les symptômes liés aux méningiomes sont en lien avec une éventuelle compression du cerveau ou de la moelle épinière/queue de cheval.
Méningiome de petite taille (peu importe sa localisation)
Lorsque le méningiome est de petite taille, il n’entraine la plupart du temps aucun symptôme (son volume est trop petit pour entrainer une compression importante du cerveau ou de la moelle épinière/queue de cheval). Il pourra être alors découvert par hasard lors de la réalisation d’un examen de radiologie réalisé pour un autre motif.
Méningiome de grande taille localisé au niveau du cerveau
Lorsque le méningiome est plus gros et localisé au niveau du cerveau, plusieurs types de symptômes peuvent survenir et s’aggraver progressivement en quelques mois/années (en lien avec l’augmentation de volume du méningiome).
L’accumulation d’une masse dans la boite crânienne va entrainer une augmentation de la pression au sein de la boite crânienne, appelée hypertension intracrânienne. Cette dernière entraine essentiellement des maux de tête (céphalées), des nausées et vomissements, et des troubles de la vision (vision double, flou visuel).
Le méningiome peut également comprimer une zone importante du cerveau (dite fonctionnelle) et ainsi empêcher cette zone de fonctionner correctement. On parle de déficit neurologique focal. Par exemple, un méningiome situé en regard de la zone du cerveau qui commande les mouvements du bras droit peut entrainer une paralysie très lentement progressive du bras droit. Ces symptômes sont très variables selon la localisation du méningiome au sein de la boite crânienne. Si le méningiome est situé à distance des zones dites fonctionnelles, aucun déficit neurologique focal ne sera observé.
Dans certains cas, le méningiome peut entrainer des crises d’épilepsie. Elles sont liées à une irritation de la surface du cerveau par le méningiome. Il existe 2 grands types de crises d’épilepsie à savoir les crises dites focales et les crises dites généralisées. Les crises focales correspondent à un déficit neurologique focal transitoire de quelques minutes avec récupération complète après la crise (ex : paralysie du bras droit pendant 20 min). Les crises généralisées correspondent à une perte de connaissance avec des mouvements des 4 membres. Un méningiome peut entrainer des crises focales, des crises généralisées ou les 2.
Méningiome de grande taille localisé au niveau de la moelle épinière/queue de cheval
Lorsque le méningiome est plus gros et localisé au niveau de la colonne vertébrale, plusieurs types de symptômes peuvent survenir et s’aggraver progressivement en quelques mois/années (en lien avec l’augmentation de volume du méningiome).
Le développement du méningiome va entrainer des douleurs au niveau de la colonne vertébrale en regard.
Le méningiome peut comprimer la moelle épinière et la faire dysfonctionner. Ceci se traduit par une difficulté pour le cerveau d’envoyer correctement des informations motrices vers les muscles (faiblesse musculaire dans les jambes et/ou les bras, impression de maladresse avec lâchage d’objet), ou par une difficulté à la peau d’envoyer des informations sensitives exactes au cerveau (engourdissements, fourmillements, sensations de membres morts, difficulté à marcher par perte d’équilibre). Parfois, il peut également exister des troubles du contrôle des urines ou des selles.
Le méningiome peut comprimer la queue de cheval et faire dysfonctionner les racines nerveuses la composant. Ceci traduire par une difficulté pour le cerveau d’envoyer correctement des informations motrices vers les muscles (faiblesse musculaire dans les jambes), ou par une difficulté à la peau d’envoyer des informations sensitives exactes au cerveau (douleurs dans les jambes, engourdissements, fourmillements). Parfois, il peut également exister des troubles du contrôle des urines ou des selles.
Bilans complémentaires à réaliser
Le diagnostic de méningiome doit être confirmé par des examens de radiologie permettant de mettre en évidence des anomalies au niveau des méninges.
Les radiographies du crâne et/ou de la colonne vertébrale n’ont que très peu d’intérêt car elles ne permettent pas de voir les méninges.
Les 2 examens permettant de visualiser un méningiome sont le scanner et l’IRM. L’IRM permet de visualiser le cerveau ou la moelle épinière/queue de cheval de manière plus précise que le scanner et est donc considérée comme l’examen de référence à réaliser.
Prise en charge
Le traitement du méningiome dépend de son volume, de sa localisation et des symptômes liés à son développement. Du fait de l’évolution très lente d’un méningiome, le traitement du méningiome n’est que rarement réalisé en urgence (sauf cas particuliers).
A l’heure actuelle, il n’existe pas vraiment de médicaments permettant de faire diminuer le volume d’un méningiome.
Une simple surveillance (avec par exemple une IRM de contrôle annuelle) peut être proposée pour les méningiomes de petite taille n’entrainant pas de symptômes particuliers.
La chirurgie est en général proposée soit pour les méningiomes de grande taille, soit pour les méningiomes qui grossissent progressivement lors des IRM de surveillance, soit lorsqu’il existe des symptômes importants en rapport avec le méningiome. La chirurgie est toujours réalisée sous anesthésie générale. Son objectif est de retirer complétement (dans la mesure du possible) le méningiome, qui sera envoyé au laboratoire pour une analyse au microscope permettant de confirmer avec certitude le diagnostic. Un suivi (en général annuel) par IRM est ensuite proposé afin de vérifier l’absence de récidive de méningiome.
L’équipe de neurochirurgie de la polyclinique Pau Pyrénées dispose de nombreux moyens de limiter les risques de l’intervention chirurgicales.
– Risque de saignement important pendant l’opération : si le méningiome est identifié comme à risque important de saignement, il est possible d’aller boucher les vaisseaux qui lui apporte le sang. Cette procédure s’appelle une embolisation. Elle est réalisée quelques jours avant l’intervention chirurgicale, au centre hospitalier de Pau, par le docteur Richter (neurologue).
– Risque de lésion du cerveau pendant l’opération : l’utilisation de la neuronavigation permet au neurochirurgien d’identifier très précisément la zone du cerveau dans laquelle se situe la tumeur (voir section technologies chirurgicales). L’utilisation du dissecteur ultrasonique cérébral permet de limiter nettement le risque de lésion du cerveau pendant l’intervention (voir section technologies chirurgicales).
– Risque lié au réveil après l’opération : dans les cas où le neurochirurgien suspecte que le réveil après anesthésie générale peut être lent et/ou difficile, le patient est transféré en réanimation au centre hospitalier de Pau immédiatement après la chirurgie. Le réveil du patient sera réalisé de manière progressive dans ce service spécialisé, sous surveillance rapprochée.
La radiothérapie (méthode qui consiste à envoyer, par le biais d’une machine, des rayons sur le méningiome pour en détruire les cellules) peut s’avérer utile dans certains cas de méningiome inopérable (leur localisation peut rendre la chirurgie trop risquée) ou après la chirurgie si celle-ci montre un retrait incomplet du méningiome ou un méningiome agressif après analyse au laboratoire.
Enfin, dans le cas très particulier des méningiomes en lien avec la prise de médicaments hormonaux, un simple arrêt des médicaments hormonaux peut suffire à faire diminuer la taille du méningiome.
Hydrocéphalie
neurochirurgiens à Pau : Expertise en Neurochirurgie dans les Pyrénées pour les Départements 64 et 65
À Pau, dans les départements des Pyrénées-Atlantiques (64) et des Hautes-Pyrénées (65), les neurochirurgiens offrent une expertise de pointe dans le traitement des affections du cerveau, de la colonne vertébrale et du système nerveux. Grâce à des technologies avancées et des techniques chirurgicales innovantes, les neurochirurgiens de Pau prennent en charge une large gamme de pathologies, allant des tumeurs cérébrales aux hernies discales en passant par la scoliose.

Ce chapitre est destiné principalement aux patients. Certaines informations médicales peuvent être légèrement simplifiées pour permettre la compréhension du grand public.
Définition
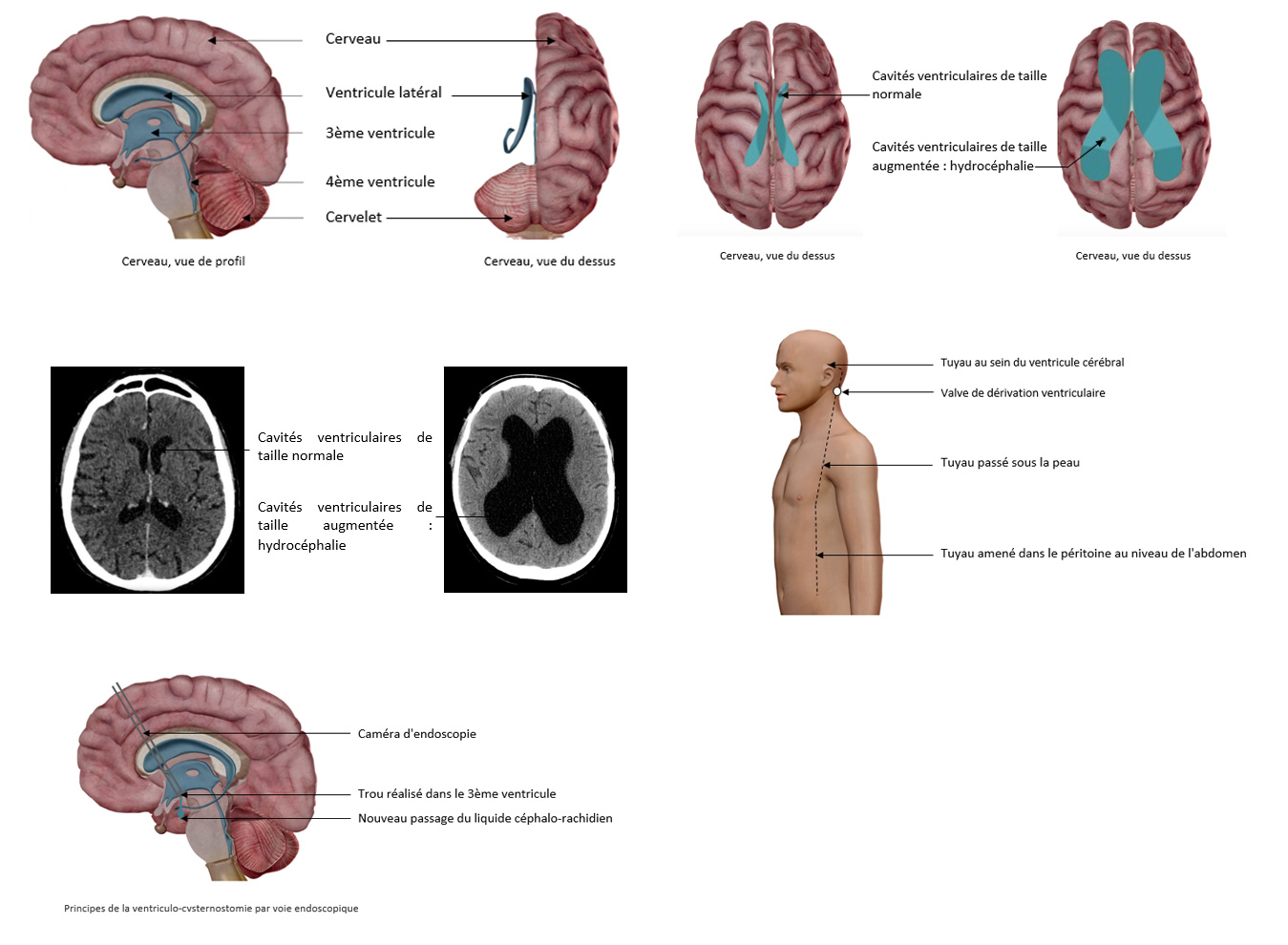
Il existe 4 cavités creuses au sein du cerveau. Ces cavités sont nommées ventricules (ou cavités ventriculaires) et communiquent entre elles. On distingue, du haut vers les bas, 2 ventricules latéraux (un de chaque côté du cerveau), un 3ème ventricule et enfin un 4ème ventricule.
Les ventricules contiennent environ 150mL d’un liquide appelé liquide céphalo-rachidien (ou liquide cérébro-spinal). Le débit de ce liquide est estimé environ à 20 mL par heure, soit 500 mL par jour chez l’adulte (Il se renouvelle 3 à 4 fois par jour).
L’hydrocéphalie correspond à une augmentation du volume des cavités ventriculaires liée à une accumulation de liquide céphalo rachidien.
Les principales causes de l’hydrocéphalie sont :
– Une obstruction sur les voies d’écoulement du liquide cérébro-spinal
– Une accumulation progressive de de liquide cérébro-spinal, le plus souvent suite à son élimination insuffisante
Symptômes et signes cliniques
Les symptômes d’hydrocéphalie associent surtout des signes en lien avec l’accumulation de liquide céphalo-rachidien au sein du cerveau et parfois des signes en lien avec la cause de l’hydrocéphalie.
L’accumulation de liquide au sein du cerveau va entrainer une augmentation de la pression au sein de la boite crânienne, appelée hypertension intracrânienne. Cette dernière entraine essentiellement des maux de tête (céphalées), des nausées et vomissements, et des troubles de la vision (vision double, flou visuel).
Les signes liés à la cause de l’hydrocéphalie sont très variables et sont souvent moins francs que les symptômes d’hypertension intracrânienne.
La vitesse d’installation des symptômes est variable et dépend également de la cause de l’hydrocéphalie. La plupart du temps, les symptômes se développement progressivement sur quelques semaines. L’augmentation progressive de la pression intracrânienne (le liquide s’accumule de plus en plus, entrainant de plus en plus de pression) fait que les symptômes ont tendance à s’accentuer avec le temps. Parfois, les symptômes s’installent de manière brutale sur quelques jours. Lorsque la pression intracrânienne devient trop importante, il peut survenir un dysfonctionnement majeur du cerveau appelé coma.
Le type d’hydrocéphalie le plus fréquent appelé hydrocéphalie à pression normale. Cette forme se retrouve surtout chez le patient de plus de 70 ans. Les symptômes associent des troubles cognitifs (problème de mémoire), des troubles sphinctériens (incontinence urinaire) et des troubles de la marche (marche à petits pas). Ces symptômes se développent de manière lente sur plusieurs mois voire années et ne sont pas à risque d’entrainer un coma.
Bilans complémentaires à réaliser
Le diagnostic d’hydrocéphalie doit être confirmé par des examens de radiologie permettant de montrer que le volume des cavités ventriculaires est augmenté.
Les radiographies du crâne n’ont que très peu d’intérêt car elles ne permettent pas de voir les cavités ventriculaires.
L’examen essentiel pour diagnostiquer cette maladie est le scanner. Il permet à la fois de prouver que les cavités ventriculaires ont un volume anormal, mais aussi de trouver la cause de l’hydrocéphalie dans la plupart des cas.
Dans les cas de diagnostic difficile, une IRM peut également être réalisée. Cet examen permet de visualiser le cerveau de manière plus précise que le scanner et ainsi de déterminer la cause de l’hydrocéphalie lorsque le scanner n’apporte pas la réponse.
Prise en charge
Le traitement de l’hydrocéphalie est le plus souvent basé sur la chirurgie (il n’existe pas de médicaments efficaces pour traiter l’hydrocéphalie). L’objectif de la chirurgie est d’enlever l’accumulation de liquide au sein des cavités ventriculaires, et ainsi de réduire la pression intracrânienne. La chirurgie est toujours réalisée sous anesthésie générale, et sera parfois réalisée en urgence en cas d’hypertension intracrânienne importante.
Il existe 4 types d’interventions chirurgicales pouvant être proposées. Le choix de l’intervention se fait selon le degré d’urgence et la cause de l’hydrocéphalie.
L’intervention la plus fréquemment réalisée consiste en la mise en place d’un tuyau reliant les cavités ventriculaires et une autre partie du corps où l’excès de liquide sera réabsorbé (cœur ou abdomen). L’ensemble du tuyau passe sous la peau et sera gardé à vie par le patient. On parle de dérivation ventriculo-cardiaque si le tuyau est dirigé vers le cœur ou de dérivation ventriculo-péritonéale si le tuyau va vers l’abdomen (et donc le péritoine). L’ensemble de ce système est relié à une valve. Il existe des valves à débit réglable et des valves à débit constant. Votre neurochirurgien évaluera le type de valve le plus adapté à votre cas particulier. Il est possible de modifier le débit de liquide céphalo rachidien qui s’écoule dans le tuyau si la valve est à débit réglable, en utilisant un aimant spécifique que l’on place au contact de la valve.
Si vous devez bénéficier d’une dérivation ventriculo-péritonéale ou dérivation ventriculo-cardiaque, votre neurochirurgien vous fournira une carte de patient porteur de valve de dérivation ventriculaire. Sur cette carte sont précisés, le type de valve et son réglage (dans le cas des valves à débit réglable). Cette carte est à garder précieusement et à présenter lors des consultations médicales en rapport avec votre hydrocéphalie.
Avec le temps il est possible que le tuyau se bouche, ne permettant alors plus de drainer l’excès de liquide céphalo-rachidien. Dans ce cas, les symptômes d’hydrocéphalie réapparaissent de manière progressive (du fait de l’accumulation progressive de liquide). Les patients porteurs d’une dérivation ventriculo-péritonéale ou ventriculo-cardiaque doivent donc bénéficier d’un suivi régulier dans un centre de neurochirurgie. Une nouvelle intervention chirurgicale sera proposée pour remplacer le tuyau bouché.
Dans les situations où l’hydrocéphalie est possiblement temporaire, le même type de chirurgie est proposé, mais le tuyau est dirigé vers une poche à l’extérieur du crâne. On parle de dérivation ventriculaire externe. Ceci évite d’implanter de manière définitive ce tuyau chez les patients qui n’en auraient besoin que quelques semaines. La surveillance du patient jusqu’au retrait du tuyau doit se faire à l’hôpital.
Dans certains cas d’hydrocéphalie liée à un blocage de l’écoulement du liquide céphalo-rachidien, il peut être proposé de réaliser une ventriculo-cysternostomie par voie endoscopique. Le principal de cette chirurgie est de perforer, à l’aide d’une caméra, le 3ème ventricule pour que l’excès de liquide passe par le trou nouvellement formé.
Enfin, dans certains cas, une chirurgie permettant de traiter la cause de l’hydrocéphalie (par exemple, retirer une lésion du cerveau qui bloque l’écoulement normal du liquide céphalo-rachidien dans les cavités ventriculaires) peut suffire à traiter l’hydrocéphalie, sans même toucher aux cavités ventriculaires.
En plus de la chirurgie, le traitement peut parfois associer la réalisation de ponctions lombaires. En effet le liquide céphalo-rachidien présent dans les cavités ventriculaires au niveau du cerveau descend le long de la colonne vertébrale jusqu’en bas du dos, où il pourra être ponctionné à l’aide d’une aiguille. Ceci est une méthode temporaire qui permet d’évacuer jusqu’à 30 à 40 mL de liquide céphalo-rachidien.
Adénome hypophysaire
Arthrodèse à Pau : Expertise en Neurochirurgie des Pyrénées
À Pau, dans les départements des Pyrénées-Atlantiques (64) et des Hautes-Pyrénées (65), l’arthrodèse est une intervention clé réalisée par les neurochirurgiens pour traiter diverses pathologies de la colonne vertébrale. Cette procédure chirurgicale, qui consiste à fusionner deux ou plusieurs vertèbres, est recommandée pour les patients souffrant de douleurs chroniques causées par des affections telles que les maladies dégénératives, les fractures ou les déformations sévères de la colonne.
L’arthrodèse est généralement envisagée lorsque les traitements conservateurs, comme la physiothérapie ou les médicaments, ne parviennent pas à soulager la douleur ou à stabiliser la colonne vertébrale. Les neurochirurgiens de Pau, au sein du Centre Hospitalier de Pau et dans les cliniques privées de la région, sont spécialisés dans cette intervention. Grâce à l’utilisation de techniques chirurgicales modernes, telles que la chirurgie mini-invasive et la navigation assistée par ordinateur, ils peuvent réduire le traumatisme opératoire et accélérer le temps de récupération.
Le but de l’arthrodèse est de stabiliser les segments vertébraux, soulager la compression des nerfs et corriger d’éventuelles déformations. Les implants, tels que des vis et des tiges métalliques, sont souvent utilisés pour maintenir les vertèbres en place pendant la fusion osseuse. Cette procédure permet aux patients de retrouver une meilleure qualité de vie en réduisant les douleurs dorsales sévères.
Pour les habitants de Pau, Tarbes et les communes environnantes des départements 64 et 65, l’accès à des soins neurochirurgicaux de qualité est facilité par la proximité de ces établissements de santé. Les patients bénéficient d’un suivi personnalisé, tant avant qu’après l’opération, ce qui favorise une réhabilitation réussie.
En résumé, l’arthrodèse pratiquée à Pau par les neurochirurgiens des Pyrénées représente une solution efficace pour les patients souffrant de pathologies vertébrales graves, offrant des résultats durables et un retour à une vie active sans douleur.

Ce chapitre est destiné principalement aux patients. Certaines informations médicales peuvent être légèrement simplifiées pour permettre la compréhension du grand public.
Définition
L’hypophyse est une glande qui secrète des hormones nécessaires au bon fonctionnement de l’organisme. Les hormones secrétées par l’hypophyse régulent entre autres le fonctionnement de la croissance, de la thyroïde, des fonctions reproductrices et de l’allaitement chez la femme.
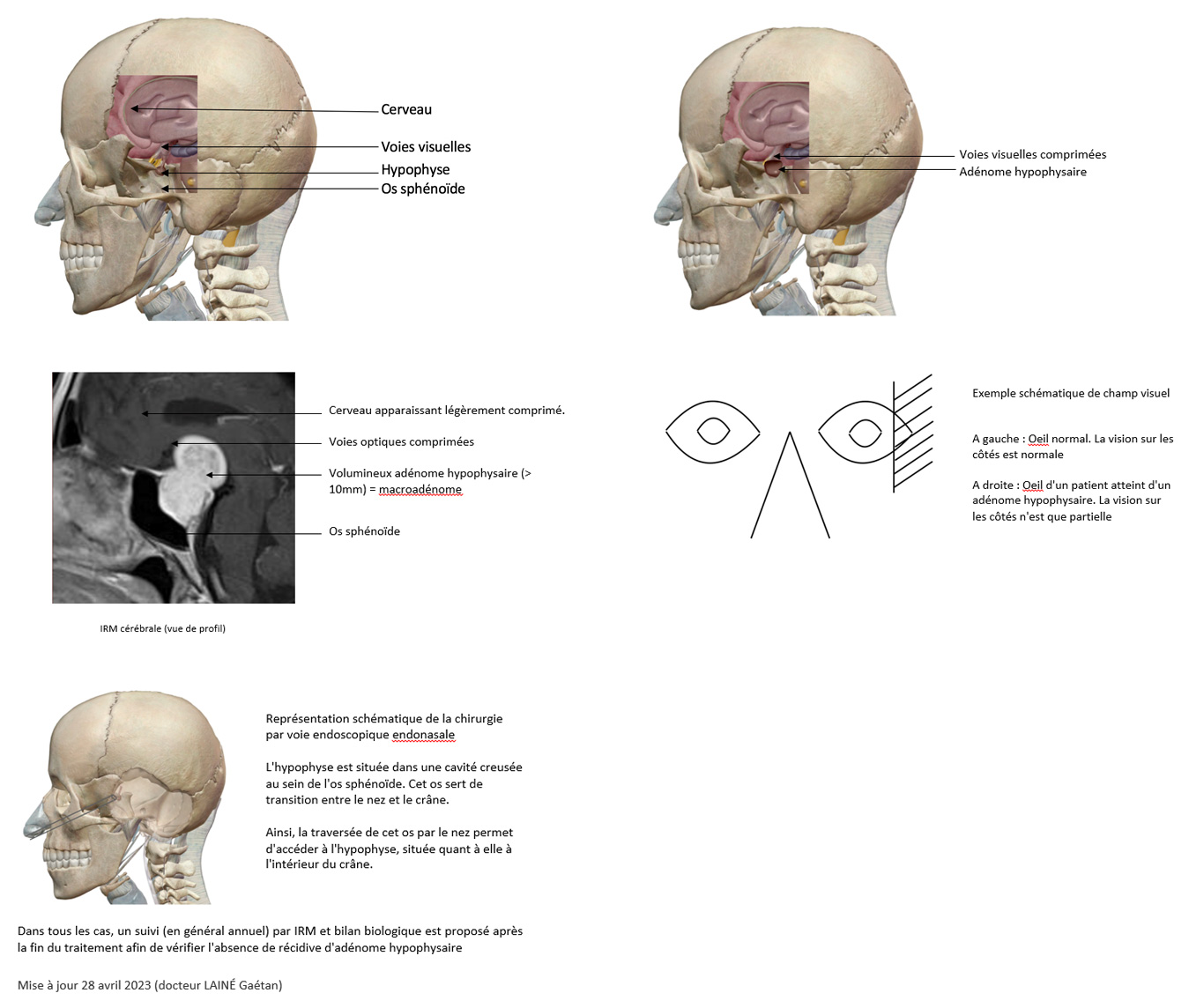
L’hypophyse se situe à l’intérieur de la boite crânienne, au sein d’une cavité creusée dans l’os sphénoïde (os faisant la jonction entre le nez, les yeux et la partie inférieure du cerveau). Ainsi, cette glande est située sous le cerveau. Les voies visuelles (qui vont du cerveau aux yeux et qui permettent de voir) sont situées juste au-dessus de l’hypophyse.
Le développement anormal de cellules dans le corps humain s’appelle une tumeur. On distingue les tumeurs dites bénignes (non agressives) des tumeurs dites malignes (agressives).
Les adénomes hypophysaires sont des tumeurs dites glandulaires (développées dans une glande). Ils correspondent à une accumulation anormale de cellules au sein de l’hypophyse, entrainant la formation d’une véritable masse de cellules. Cette masse va perturber le fonctionnement normal de l’hypophyse (et donc perturber la sécrétion des hormones de l’hypophyse) et peut, si elle est volumineuse, comprimer les voies visuelles entrainant des troubles de la vision.
Les adénomes hypophysaires sont dans la plupart des cas des tumeurs bénignes, dont la croissance lente se fait sur plusieurs mois/années. Des études récentes ont montré que 10% de la population adulte présenterait un adénome hypophysaire. Dans la majorité des cas, cet adénome n’entrainera aucun trouble tout au long de la vie.
Symptômes et signes cliniques
Lorsque l’adénome est de petite taille, il n’entraine la plupart du temps aucun symptôme. Il pourra être alors découvert par hasard lors de la réalisation d’un examen de radiologie réalisé pour un autre motif.
Les symptômes liés aux adénomes hypophysaires comprennent à des degrés variables des signes hormonaux (par perturbation de la sécrétion normale des hormones par l’hypophyse) et des troubles visuels (en lien avec la compression des voies optiques). L’ensemble de ces symptômes se développent de manière lentement progressive sur plusieurs mois/années.
Les atteintes hormonales correspondent la plupart du temps à un excès d’une hormone secrétée par l’hypophyse. Les symptômes sont extrêmement variés et peuvent correspondre à un amaigrissement, une nervosité importante, une accélération du rythme cardiaque (excès d’hormone thyroïdienne, aussi appelée hyperthyroïdie), une augmentation progressive de la taille sur plusieurs années (excès d’hormone de croissance, aussi appelée acromégalie), écoulement de lait par les mamelons, troubles des règles, troubles sexuels (excès de prolactine, aussi appelée hyperprolactinémie), une fonte des muscles, prise de poids au niveau du ventre, apparition de vergetures (excès de cortisol, aussi appelé hypercorticisme), ou encore une diminution de la libido, des troubles de l’érection ou des règles (excès d’hormones sexuelles). Dans de rare cas, les adénomes hypophysaires entrainent une baisse des hormones sécrétées par l’hypophyse. On parle d’insuffisance hypophysaire, qui se caractérise par une fatigue importante, une pâleur, une fragilisation de la peau qui devient fine.
Les troubles visuels rencontrés dans les adénomes hypophysaires correspondent un rétrécissement du champ visuel prédominant sur les côtés (autrement dit, il devient de plus en plus difficile de voir ce qui n’est pas droit devant soi). Dans les cas d’atteinte très sévère (compression importante et prolongée pendant plusieurs semaines/mois), la capacité à voir correctement peut être nettement altérée jusqu’à être quasiment aveugle (dans certains cas exceptionnels).
Rarement, le développement d’un adénome hypophysaire très volumineux va entrainer une augmentation de la pression au sein de la boite crânienne, appelée hypertension intracrânienne. Cette dernière entraine essentiellement des maux de tête (céphalées), des nausées et vomissements, et des troubles de la vision (vision double, flou visuel).
Il existe également de rares cas où l’adénome grossit de manière brutale (à l’occasion d’un saignement à l’intérieur de l’adénome). On parle d’apoplexie hypophysaire. Les symptômes les plus fréquents en sont des maux de tête importants de survenue brutale, des troubles de la vision brutaux et sévères (par compression importante et brutale des voies visuelles) et des troubles en lien avec la perturbation des sécrétions hormonales de l’hypophyse.
Bilans complémentaires à réaliser
Le diagnostic d’adénome hypophysaire doit être confirmé par des examens de biologie (prise de sang) permettant de savoir quelle hormone est trop/pas assez sécrétée par l’hypophyse atteinte, des examens de radiologie permettant de visualiser l’adénome et des examens de la vision pour voir s’il existe un retentissement de l’adénome sur le champ visuel.
L’équipe de neurochirurgie travaille de manière conjointe avec les différents endocrinologues de la région (centre hospitalier de Pau, clinique d’Aressy, clinique Princess) dans le bilan de l’adénome hypophysaire.
La prise de sang étudiera les valeurs des principales hormones sécrétées par l’hypophyse (ACTH, TSH, FSH/LH, IGF1, prolactine) ainsi que le cortisol et les hormones thyroïdiennes, en les comparant aux valeurs dites normales (normes définies chez les sujets sains, sans adénome hypophysaire). Les résultats seront analysés par les équipes d’endocrinologie.
Les radiographies du crâne n’ont que très peu d’intérêt car elles ne permettent pas de voir les cavités ventriculaires. Un scanner du cerveau peut permettre de découvrir un adénome hypophysaire. L’examen de référence à réaliser reste tout de même une IRM du cerveau, qui permet de visualiser le cerveau et les voies optiques de manière plus précise que le scanner. On parle de microadénome lorsque celui-ci mesure moins de 10mm et de macroadénome lorsqu’il mesure plus de 10 mm.
Les examens de la vision réalisées dans le cas d’un adénome hypophysaire sont l’acuité visuelle (évalue la qualité de la vision sur 10), le champ visuel (évalue l’espace environnant perçu par l’œil lorsque l’on regarde droit devant), le fond d’oeil et l’OCT (ces 2 examens permettent d’établir des valeurs pronostiques sur la vision).
Prise en charge
La prise en charge d’un adénome hypophysaire est dite multidisciplinaire, car elle fait intervenir plusieurs types de médecins spécialistes (endocrinologue, ophtalmologue, neuroradiologue, neurochirurgien, radiothérapeute).
Le but du traitement d’un adénome hypophysaire est double : faire diminuer la taille de l’adénome hypophysaire et traiter les symptômes liés aux modifications du taux d’hormones. Du fait de l’évolution très lente d’un adénome hypophysaire, le traitement n’est que rarement réalisé en urgence (sauf dans certains cas particuliers comme par exemple l’apoplexie hypophysaire).
Une simple surveillance (avec par exemple une IRM de contrôle et un bilan biologique annuel) peut être proposée pour les adénomes hypophysaires de petite taille n’entrainant pas de symptômes particuliers.
Pour les autres cas d’adénome hypophysaire, le traitement repose sur une concertation entre neurochirurgien et endocrinologue. Certains types d’adénome (notamment les adénomes à prolactine) peuvent régresser de manière rapide et importante en utilisant des médicaments. Lorsque l’adénome ne risque pas de régresser avec un traitement par médicaments, une chirurgie peut être proposée. L’intervention est réalisée la plupart du temps par voie endoscopique endonasale (autrement dit, à l’aide d’une caméra insérée dans le nez), sous anesthésie générale. Son objectif est de retirer complétement (dans la mesure du possible) l’adénome, qui sera envoyé au laboratoire pour une analyse au microscope permettant de confirmer avec certitude le diagnostic. L’utilisation pendant l’opération de la neuronavigation permet au neurochirurgien de localiser avec précision l’adénome (voir section technologies chirurgicales).
Dans tous les cas, un suivi (en général annuel) par IRM et bilan biologique est proposé après la fin du traitement afin de vérifier l’absence de récidive d’adénome hypophysaire.